Una domanda sul pH delle creme!
Moderatori: gigetta, Laura, tagliar, Bimba80
-
michelle

- utente avanzato

- Messaggi: 1267
- Iscritto il: 30/09/2014, 9:31
- Località: tra CR e PC
Re: Una domanda sul pH delle creme!
Ho fatto una grande cazzata.
Ieri ho fatto una crema viso da notte, bella grassa, emulsionata a caldo, ben riuscita, tutto ok.
Arrivo alla fine con la regolazione del ph e vedo che è altino, a 7. Allora procedo con l'acido lattico per abbassarlo e rimisuro, ma non è ancora a posto, quindi altro acido lattico e via così per altre due volte.
Quando le cartine mi assumono colori mai visti prima mi rendo conto che non stavo usando il lattico, ma la soda.
E ci credo che non scendeva!
Se aggiungo lattico salvola crema o è da buttare? Solitamente non sono così imbecille.
Ieri ho fatto una crema viso da notte, bella grassa, emulsionata a caldo, ben riuscita, tutto ok.
Arrivo alla fine con la regolazione del ph e vedo che è altino, a 7. Allora procedo con l'acido lattico per abbassarlo e rimisuro, ma non è ancora a posto, quindi altro acido lattico e via così per altre due volte.
Quando le cartine mi assumono colori mai visti prima mi rendo conto che non stavo usando il lattico, ma la soda.
E ci credo che non scendeva!
Se aggiungo lattico salvola crema o è da buttare? Solitamente non sono così imbecille.
-
Lola
- Grande Capa

- Messaggi: 48775
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
Re: Una domanda sul pH delle creme!
Cosa fa soda caustica + acido lattico?
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
michelle

- utente avanzato

- Messaggi: 1267
- Iscritto il: 30/09/2014, 9:31
- Località: tra CR e PC
Re: Una domanda sul pH delle creme!
sodio lattato. credo.
-
Lola
- Grande Capa

- Messaggi: 48775
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
Re: Una domanda sul pH delle creme!
Brava. Ed è nocivo sulla pelle?
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
michelle

- utente avanzato

- Messaggi: 1267
- Iscritto il: 30/09/2014, 9:31
- Località: tra CR e PC
Re: Una domanda sul pH delle creme!
Per niente. Anzi. Però avevo paura di aver combinato un danno perchè non avevo rispettato nessuna precisa proporzione.
Quindi posso spalmare in tranquillità..
Quindi posso spalmare in tranquillità..
-
Lola
- Grande Capa

- Messaggi: 48775
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
Re: Una domanda sul pH delle creme!
esatto, se alla prova delle cartine il pH è a posto significa che tutto il resto che avanza è sodio lattato e male non fa.
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
michelle

- utente avanzato

- Messaggi: 1267
- Iscritto il: 30/09/2014, 9:31
- Località: tra CR e PC
Re: Una domanda sul pH delle creme!
Grazie Lola. La tua maieutica è sempre molto efficace.
-
Mama80

- novellino

- Messaggi: 6
- Iscritto il: 15/03/2017, 0:27
- Località: Milano
Re: Una domanda sul pH delle creme!
Ehm, ciao a tutti....domandina ulteriore: a me è successa più o meno la stessa cosa di Michelle, ora il mio dubbio è, ma il fatto di aver portato per sbaglio a PH 14 una preparazione anche se per poco tempo, non rischia di rovinare l'efficacia degli ingredienti usati? Io ho messo alcuni attivi tipo bava di lumaca, nanoliposomi multivitaminici, skin revit di GC...se poi porto a PH 6 non ho veramente rovinato o invalidato nulla? Grazie!
-
Lola
- Grande Capa

- Messaggi: 48775
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
Re: Una domanda sul pH delle creme!
Se é per pochissimo tempo é difficile aver fatto grandi danni, per le reazioni chimiche ci vuole grande potenza o tanto tempo o calore. Il pH a 14 é la grande potenza, manca il tempo e il calore. Ammesso che fosse veramente 14, per arrivarci occorrono vagonate di soda e le cartine da quelle parti non sono così chiare. Certo dovresti chiarire quanto tempo è passato e come sei riuscita ad arrivare a quel pH.
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
Mama80

- novellino

- Messaggi: 6
- Iscritto il: 15/03/2017, 0:27
- Località: Milano
Re: Una domanda sul pH delle creme!
Allora, stavo facendo una prova di latte antismagliature perchè non ero sicura della ricetta, per cui ne ho fatti 50g. Il ph era 4.5 e per il Salvacosm diceva che era meglio portarlo a 6. Allora ho aggiunto Sodio idrossido 30% (è quello che ho)...mi ricordavo che ce ne voleva un bel po' per alzare il ph, ma erroneamente perchè l'avevo sperimentato un bel po' di tempo fa su quantità ben maggiori (tipo 250g di crema) e con sodio idrossido al 10%...Fatto sta che ne ho messe 4 o 5 gocce e il PH è schizzato 
Nel giro di un paio di minuti ho recuperato con l'acido lattico, ma non so se è stato sufficiente per salvare il tutto
Errori da principiante
Nel giro di un paio di minuti ho recuperato con l'acido lattico, ma non so se è stato sufficiente per salvare il tutto
Errori da principiante
-
SsilviaA

- Spignattatrice

- Messaggi: 9550
- Iscritto il: 27/01/2015, 10:16
- Località: Hogwarts
Re: Una domanda sul pH delle creme!
Beh si, hai inserito tanta soda in più della prima volta che hai descitto, è normale. Anche avessi avuto un pH 2 iniziale sarebbe schizzato alle stelle  credo che 2-3 minuti si possa considerare "poco tempo", ma se vuoi aspettare conferma...
credo che 2-3 minuti si possa considerare "poco tempo", ma se vuoi aspettare conferma...
Io il tempo non lo capisco proprio, da un po' di tempo mi chiedo una cosa. Prendiamo in esame grande potenza + tempo, che dovrebbe creare una reazione come da te descritto Lola. Diciamo che sta crema sta a pH 14 per 1 mese, cos'è che fa scattare la reazione a livello teorico? Cioè, perchè succede "dopo" e non "prima"? In linea generale, perchè le reazioni chimiche hanno delle tempistiche? L'atomo ha un cervello/impulso e decide spontaneamente e consapevolmente di interagire con un altro? Bisogna aspettare che l'atomo casualmente sbatta contro l'altro?
Sono off topic vero..?
Io il tempo non lo capisco proprio, da un po' di tempo mi chiedo una cosa. Prendiamo in esame grande potenza + tempo, che dovrebbe creare una reazione come da te descritto Lola. Diciamo che sta crema sta a pH 14 per 1 mese, cos'è che fa scattare la reazione a livello teorico? Cioè, perchè succede "dopo" e non "prima"? In linea generale, perchè le reazioni chimiche hanno delle tempistiche? L'atomo ha un cervello/impulso e decide spontaneamente e consapevolmente di interagire con un altro? Bisogna aspettare che l'atomo casualmente sbatta contro l'altro?
Sono off topic vero..?
𝓛𝓾𝓶𝓸𝓼  𝓽𝓸 𝓼𝓱𝓮𝓭 𝓵𝓲𝓰𝓱𝓽 𝓸𝓷 𝓮𝓿𝓮𝓻𝔂𝓽𝓱𝓲𝓷𝓰
𝓽𝓸 𝓼𝓱𝓮𝓭 𝓵𝓲𝓰𝓱𝓽 𝓸𝓷 𝓮𝓿𝓮𝓻𝔂𝓽𝓱𝓲𝓷𝓰
-
tagliar

- Moderatrice VIP

- Messaggi: 20018
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
Re: Una domanda sul pH delle creme!
Brevemente, ogni reazione chimica procede più o meno speditamente secondo alcuni "parametri": il profilo termodinamico della reazione e la sua cinetica, oltre all'utilizzo di catalizzatori (ma non è il nostro caso) e alla superficie di contatto dei reagenti.
Ora mi spiego meglio:
- profilo termodinamico: si tratta di una curva tipo questa (blu o verde non importa):
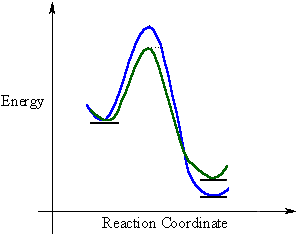
dove al posto di "reaction coordinate" puoi sostituire il parametro tempo.
Immagina di dover superare un dislivello: se è piccolo (una collinetta) ci impiegherai poco tempo e l'energia spesa sarà poca; se si tratta del Monte Bianco, ci impiegherai di più e ti servirà ben più energia per farlo.
E' quello che avviene alle reazioni chimiche: devono superare un dislivello (la parte più alta della curva) per poter avvenire e per farlo bisogna fornire energia (poca o tanta dipende da quanto è alto il "picco" della curva, quindi dal tipo di reazione, e i catalizzatori aumentano la velocità di una reazione perché abbassano il picco).
- cinetica: la cinetica, ovvero la velocità di una reazione a parità di energia fornita, può dipendere anche dalla concentrazione dei reagenti; può perché esistono reazioni a cinetica zero, ovvero che non dipendono da tale concentrazione, ma esistono anche reazioni a cinetica uno (la velocità dipende dalla concentrazione di un solo reagente con esponente 1), cinetica due (la velocità dipende dalla concentrazione di uno o più reagenti in modo che la somma degli esponenti sia pari a 2) o anche di cinetica superiore a due.
Ora mi spiego meglio:
- profilo termodinamico: si tratta di una curva tipo questa (blu o verde non importa):

dove al posto di "reaction coordinate" puoi sostituire il parametro tempo.
Immagina di dover superare un dislivello: se è piccolo (una collinetta) ci impiegherai poco tempo e l'energia spesa sarà poca; se si tratta del Monte Bianco, ci impiegherai di più e ti servirà ben più energia per farlo.
E' quello che avviene alle reazioni chimiche: devono superare un dislivello (la parte più alta della curva) per poter avvenire e per farlo bisogna fornire energia (poca o tanta dipende da quanto è alto il "picco" della curva, quindi dal tipo di reazione, e i catalizzatori aumentano la velocità di una reazione perché abbassano il picco).
- cinetica: la cinetica, ovvero la velocità di una reazione a parità di energia fornita, può dipendere anche dalla concentrazione dei reagenti; può perché esistono reazioni a cinetica zero, ovvero che non dipendono da tale concentrazione, ma esistono anche reazioni a cinetica uno (la velocità dipende dalla concentrazione di un solo reagente con esponente 1), cinetica due (la velocità dipende dalla concentrazione di uno o più reagenti in modo che la somma degli esponenti sia pari a 2) o anche di cinetica superiore a due.

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)
-
Lola
- Grande Capa

- Messaggi: 48775
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
Re: Una domanda sul pH delle creme!
Come spieghi bene le cose Tagliar 
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
Mama80

- novellino

- Messaggi: 6
- Iscritto il: 15/03/2017, 0:27
- Località: Milano
Re: Una domanda sul pH delle creme!
Che meraviglia! È davvero interessante il mondo della chimica...peccato non averla studiata meglio all’università! Grazie per la spiegazione!
-
SsilviaA

- Spignattatrice

- Messaggi: 9550
- Iscritto il: 27/01/2015, 10:16
- Località: Hogwarts
Re: Una domanda sul pH delle creme!
Grazie tagliar del tuo tempo 
Molto chiaro! Però non riesco ad immaginarlo. Cos'è nella realtà il dislivello? E per energia fornita cosa intendi? Riesco a pensare solo al calore, ma se non hai usato questo termine credo che ci sia un motivo.tagliar ha scritto: Immagina di dover superare un dislivello: se è piccolo (una collinetta) ci impiegherai poco tempo e l'energia spesa sarà poca; se si tratta del Monte Bianco, ci impiegherai di più e ti servirà ben più energia per farlo.
E' quello che avviene alle reazioni chimiche: devono superare un dislivello (la parte più alta della curva) per poter avvenire e per farlo bisogna fornire energia (poca o tanta dipende da quanto è alto il "picco" della curva, quindi dal tipo di reazione, e i catalizzatori aumentano la velocità di una reazione perché abbassano il picco).
𝓛𝓾𝓶𝓸𝓼  𝓽𝓸 𝓼𝓱𝓮𝓭 𝓵𝓲𝓰𝓱𝓽 𝓸𝓷 𝓮𝓿𝓮𝓻𝔂𝓽𝓱𝓲𝓷𝓰
𝓽𝓸 𝓼𝓱𝓮𝓭 𝓵𝓲𝓰𝓱𝓽 𝓸𝓷 𝓮𝓿𝓮𝓻𝔂𝓽𝓱𝓲𝓷𝓰
-
tagliar

- Moderatrice VIP

- Messaggi: 20018
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
Re: Una domanda sul pH delle creme!
Il dislivello è l'aumento di energia che bisogna fornire al sistema affinchè si inneschi la reazione (nel grafico è la differenza tra l'energia del picco e l'energia dei reagenti che è quel tratto orizzontale a sinistra del grafico).
L'energia fornita può essere di tanti tipi: la più comune è il calore, ma ci sono reazioni che si innescano con la sola agitazione meccanica (come accade con la nitroglicerina, che esplode per semplice scuotimento del contenitore che la contiene), altre che si innescano con la radiazione (es. gli UV che induriscono alcuni smalti per unghie, la luce che innesca la fotosintesi) e altre che avvengono sotto l'effetto di energia elettrica (es. le reazioni elettrochimiche).
L'energia fornita può essere di tanti tipi: la più comune è il calore, ma ci sono reazioni che si innescano con la sola agitazione meccanica (come accade con la nitroglicerina, che esplode per semplice scuotimento del contenitore che la contiene), altre che si innescano con la radiazione (es. gli UV che induriscono alcuni smalti per unghie, la luce che innesca la fotosintesi) e altre che avvengono sotto l'effetto di energia elettrica (es. le reazioni elettrochimiche).

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)