Chelanti
Moderatori: gigetta, Laura, tagliar, MissBarbara
Regole del forum
in questa sezione NON SI POSTANO INCI
in questa sezione NON SI POSTANO INCI
-
fla~
- utente avanzato

- Messaggi: 191
- Iscritto il: 26/12/2007, 23:58
- Località: Roma
Chelanti
Cosa vuol dire chelante? 
-
Lola
- Grande Capa

- Messaggi: 49357
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
sequestrante: acchiappa gli ioni vaganti, che di solito derivano dai metalli, che si attaccherebbero al tuo olio innestando la reazione chimica che porta all'irrancidimento.
Ultima modifica di Lola il 23/11/2010, 17:42, modificato 2 volte in totale.
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
tagliar

- Moderatrice VIP

- Messaggi: 20084
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
Aggiungo a quello che ha detto Lola...fla~ ha scritto:Ora seriamente, cosa vuol dire chelante?
Il sequestrante è una molecola in grado di legare ioni o atomi, in modo da formare complessi più o meno stabili.
In questo modo, lo ione o atomo viene eliminato (sequestrato) dalla soluzione e non può partecipare ad eventuali reazioni.
Un esempio è l'EDTA che è formato da due parti che legano ioni calcio e magnesio come si trattasse delle chele di un granchio che "pinzano qualcosa": questi ioni vengono quindi sottratti dalla soluzione e non possono partecipare ad eventuali reazioni, che spesso sono reazioni di degradazione ad opera di enzimi, in quanto tali enzimi per lavorare hanno bisogno di questi ioni.
L'EDTA viene anche usato per rendere meno dura l'acqua e ridurre la formazione di calcare (carbonato di calcio)
hai presente le chele di un granchio che si chiudono a pinza?
Un chelante è una molecola che si comporta in maniera simile, cioè ha due parti che si "chiudono" legando di solito uno ione (o un atomo) e formando un complesso molto stabile dal quale lo ione non si dissocia: praticamente sottrai lo ione dalla soluzione perchè si lega al chelante e non interagisce più con altri ioni o molecole in soluzione.
Un esempio classico di chelante è l'EDTA (acido etilendiamminotetracetico):
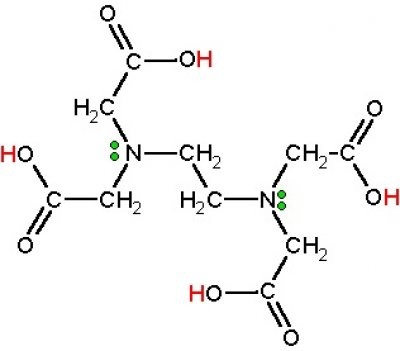
gli H in rosso sono idrogeni acidi, quindi si dissociano lasciando il gruppo COO- che lega appunto ioni positivi come lo zinco.
Un esempio di struttura che si forma è questa, dove intervengono anche gli atomi di azoto (e dove M sta per l'atomo chelato):
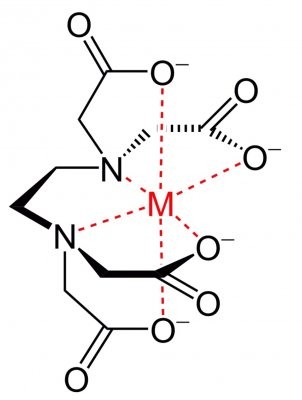

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)
-
Vati

- Spignattatrice Esperta

- Messaggi: 1002
- Iscritto il: 04/11/2008, 23:42
- Località: Pisa
-
tagliar

- Moderatrice VIP

- Messaggi: 20084
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
-
anto
- Spignattatore Esperto

- Messaggi: 5171
- Iscritto il: 03/10/2006, 9:54
-
tagliar

- Moderatrice VIP

- Messaggi: 20084
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
Chelanti e antiossidanti sono categorie diverse di sostanze.
I chelanti sottraggono ioni o molecole dalla soluzione (ho già spiegato il meccanismo qui sopra), mentre gli antiossidanti sono molecole che si ossidano più facilmente di altre, quindi impediscono l'ossidazione di altre sostanze perchè prima si ossidano loro (è tutta una questione di potenziali ossidativi, ma qui la cosa si fa più complicata).
Che poi i chelanti siano utili per impedire certe ossidazioni è vero, perchè spesso il meccanismo ossidativo è accelerato dalla presenza di metalli, che i chelanti sottraggono alla soluzione, però non definirei i chelanti come degli antiossidanti veri e propri.
I chelanti sottraggono ioni o molecole dalla soluzione (ho già spiegato il meccanismo qui sopra), mentre gli antiossidanti sono molecole che si ossidano più facilmente di altre, quindi impediscono l'ossidazione di altre sostanze perchè prima si ossidano loro (è tutta una questione di potenziali ossidativi, ma qui la cosa si fa più complicata).
Che poi i chelanti siano utili per impedire certe ossidazioni è vero, perchè spesso il meccanismo ossidativo è accelerato dalla presenza di metalli, che i chelanti sottraggono alla soluzione, però non definirei i chelanti come degli antiossidanti veri e propri.

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)
-
sushi

- Spignattatrice scientifica

- Messaggi: 1406
- Iscritto il: 29/07/2010, 21:52
Tiro su per chiedere lumi agli esperti (credo che arriverà Tagliar): qual'è, parlando di "forza" chelante, la differenza fra il monosodio citrato, disodio citrato e trisodio citrato? Ho cercato su internet e tutti e tre risultano essere usati (anche) come chelanti, ma nessuna info più dettagliata.
Nie jest łatwo pojąć nawet to
to że co rano słońce świeci
że świat będzie jakim stworzą go
niepoczęte jeszcze dzieci.
(Piotr Rubik, Strażnik raju)
to że co rano słońce świeci
że świat będzie jakim stworzą go
niepoczęte jeszcze dzieci.
(Piotr Rubik, Strażnik raju)
-
tagliar

- Moderatrice VIP

- Messaggi: 20084
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
Nessuna.
E' la parte "citrato" che chela, quindi più l'ambiente è basico più citrato c'è, ma questo non fluisce sulla forza chelante ma su quanto citrato c'è che può chelare.
Quando tu metti uno qualsiasi dei sali che hai nominato in acqua, il sale si scinde in ione sodio (che non ha nessun effetto se non quello di modificare il pH alzandolo) e citrato, che è un mix di tutte le forme di citrato, ovvero* A3-, HA2-, H2A- e H3A, che dipende dal pH al quale sei.
Più il pH è alto e più A3- c'è, quindi più molecole chelanti ci sono, ma A3- può derivare da uno qualsiasi dei sali nominati.
spero di essermi spiegata
*con A si intende la parte della molecola a cui sono legati gli H acidi
E' la parte "citrato" che chela, quindi più l'ambiente è basico più citrato c'è, ma questo non fluisce sulla forza chelante ma su quanto citrato c'è che può chelare.
Quando tu metti uno qualsiasi dei sali che hai nominato in acqua, il sale si scinde in ione sodio (che non ha nessun effetto se non quello di modificare il pH alzandolo) e citrato, che è un mix di tutte le forme di citrato, ovvero* A3-, HA2-, H2A- e H3A, che dipende dal pH al quale sei.
Più il pH è alto e più A3- c'è, quindi più molecole chelanti ci sono, ma A3- può derivare da uno qualsiasi dei sali nominati.
spero di essermi spiegata
*con A si intende la parte della molecola a cui sono legati gli H acidi

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)
-
sushi

- Spignattatrice scientifica

- Messaggi: 1406
- Iscritto il: 29/07/2010, 21:52
Grazie Tagliar! Quindi se ho capito bene, in poche parole un grammo di sodio citrato (sia mono- o di- o tri-) in soluzione a pH basso chela meno di un grammo di sodio citrato a pH alto perché forma meno parti "libere" di citrato che chelano? Giusto?
Ma c'è una qualche tabella indicativa che dice quanto, o meglio, quale percentuale, è chelante di un grammo di sodio citrato a pH diversi? Per esempio, che ne so, a pH 5 solo il 30% è chelante, il resto è in forma di H3A; a pH 7 è chelante il 50% e così via. Esiste qualcosa di simile?
E poi ultima: una molecola di citrato A3- chela un atomo con valore 3+, HA2- un atomo con valore 2+ e così via?
p.s.: scusa se non ho usato la terminologia esatta ma già in lingua madre mi è difficile capire qualcosa di chimica, figuriamoci in italiano!
Ma c'è una qualche tabella indicativa che dice quanto, o meglio, quale percentuale, è chelante di un grammo di sodio citrato a pH diversi? Per esempio, che ne so, a pH 5 solo il 30% è chelante, il resto è in forma di H3A; a pH 7 è chelante il 50% e così via. Esiste qualcosa di simile?
E poi ultima: una molecola di citrato A3- chela un atomo con valore 3+, HA2- un atomo con valore 2+ e così via?
p.s.: scusa se non ho usato la terminologia esatta ma già in lingua madre mi è difficile capire qualcosa di chimica, figuriamoci in italiano!
Nie jest łatwo pojąć nawet to
to że co rano słońce świeci
że świat będzie jakim stworzą go
niepoczęte jeszcze dzieci.
(Piotr Rubik, Strażnik raju)
to że co rano słońce świeci
że świat będzie jakim stworzą go
niepoczęte jeszcze dzieci.
(Piotr Rubik, Strażnik raju)
-
tagliar

- Moderatrice VIP

- Messaggi: 20084
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
sushi, ma qual è la tua lingua madre? 
Io avrei detto l'italiano!!
una mole di sodio citrato (sia mono- o di- o tri-) in soluzione a pH basso chela meno di una mole di sodio citrato a pH alto perché forma meno parti "libere" di citrato che chelano
* mole = g/PM
Mi riprometto di andare a vedere, ma mi sembra di ricordare che non sia un semplice legame ionico a dare il chelato, ma ci sono di mezzo altri legami che coinvolgono il doppietto elettronico libero dell'atomo di ossigeno.
Io avrei detto l'italiano!!
Non è corretto parlare di grammi, perchè 1 g dei 3 sali contiene un diverso numero di molecole (bisogna rapportarsi al peso molecolare (PM) delle 3 specie, quindi si deve ragionare in termini di moli*), comunque la tua frase corretta sarebbe:sushi ha scritto:Grazie Tagliar! Quindi se ho capito bene, in poche parole un grammo di sodio citrato (sia mono- o di- o tri-) in soluzione a pH basso chela meno di un grammo di sodio citrato a pH alto perché forma meno parti "libere" di citrato che chelano? Giusto? [/size]
una mole di sodio citrato (sia mono- o di- o tri-) in soluzione a pH basso chela meno di una mole di sodio citrato a pH alto perché forma meno parti "libere" di citrato che chelano
* mole = g/PM
No, non esistono tabelle, ma si può calcolare a tavolino sapendo i valori delle costanti di dissociazione delle varie forme dell'acido citrico (il che non è semplicissimo perchè si tratta di tener conto di 3 costanti acide, quindi bisogna risolvere un sistema a 5 variabili).sushi ha scritto:Ma c'è una qualche tabella indicativa che dice quanto, o meglio, quale percentuale, è chelante di un grammo di sodio citrato a pH diversi? Per esempio, che ne so, a pH 5 solo il 30% è chelante, il resto è in forma di H3A; a pH 7 è chelante il 50% e così via. Esiste qualcosa di simile?
Qui dovrei andare a rivedere qualche libro, ma se non ricordo male è la forma A3- che chela, non so quanto lo faccia la forma HA2- (a ben vedere però gli ioni tipo Ca2+ e Mg2+ non hanno bisogno di più cariche per essere chelati) e comunque le altre forme non chelano nulla.sushi ha scritto:E poi ultima: una molecola di citrato A3- chela un atomo con valore 3+, HA2- un atomo con valore 2+ e così via?
Mi riprometto di andare a vedere, ma mi sembra di ricordare che non sia un semplice legame ionico a dare il chelato, ma ci sono di mezzo altri legami che coinvolgono il doppietto elettronico libero dell'atomo di ossigeno.

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)
-
sushi

- Spignattatrice scientifica

- Messaggi: 1406
- Iscritto il: 29/07/2010, 21:52
Non sono italiana, sono slovena... quindi mi scuso in anticipo sia per gli errori di ortografia che di terminologia (soprattutto mi scuso per i grammi e le moli).tagliar ha scritto:sushi, ma qual è la tua lingua madre?
Io avrei detto l'italiano!!
Non so se questo c'entra o non c'entra ma rivedendo le varie formule di citrati (magnesio citrato, calcio citrato, citrato di ferro, zinco citrato etc) vedo che anche se tutti gli ioni sono di tipo 2+ ci vuole un numero di anioni di citrato diverso per farli legare. E in più sembra che ci voglia anche il tipo di aniono diverso. Ma io non mi intendo di chimica, quindi avrei potuto anche capire male...tagliar ha scritto:Qui dovrei andare a rivedere qualche libro, ma se non ricordo male è la forma A3- che chela, non so quanto lo faccia la forma HA2- (a ben vedere però gli ioni tipo Ca2+ e Mg2+ non hanno bisogno di più cariche per essere chelati) e comunque le altre forme non chelano nulla.sushi ha scritto:E poi ultima: una molecola di citrato A3- chela un atomo con valore 3+, HA2- un atomo con valore 2+ e così via?
Vedo che la cosa è ben più complicata di quanto pensavo... Siccome gli altri chelanti mi sono irraggiungibili pensavo di provare ad usare il sodio citrato come chelante (anche se Anto dice che non è abbastanza forte ma io son testarda). A questo punto credo che ci dovrò rinuncare.tagliar ha scritto:No, non esistono tabelle, ma si può calcolare a tavolino sapendo i valori delle costanti di dissociazione delle varie forme dell'acido citrico (il che non è semplicissimo perchè si tratta di tener conto di 3 costanti acide, quindi bisogna risolvere un sistema a 5 variabili).
Nie jest łatwo pojąć nawet to
to że co rano słońce świeci
że świat będzie jakim stworzą go
niepoczęte jeszcze dzieci.
(Piotr Rubik, Strażnik raju)
to że co rano słońce świeci
że świat będzie jakim stworzą go
niepoczęte jeszcze dzieci.
(Piotr Rubik, Strażnik raju)
-
laura85la
- utente
- Messaggi: 32
- Iscritto il: 18/09/2010, 13:01
- Località: Cesena
Re: Chelanti
ho trovato questo agente chelante "Sodium Phytate" in una pasta all'ossido di zinco,quindi se ho capito bene in questo caso è stato utilizzato con lo scopo di rende più stabile la pasta e per ritardarne l'ossidazione ?
se volessi riprodurla senza mettere il chelante rischierei qualcosa?
se volessi riprodurla senza mettere il chelante rischierei qualcosa?
-
tagliar

- Moderatrice VIP

- Messaggi: 20084
- Iscritto il: 29/09/2006, 9:57
- Località: Milano
Re: Chelanti
Potrebbe essere usato per chelare lo zinco che va in soluzione, in modo che non alteri il pH della preparazione.

“Siate felici e se qualche volta la felicità si scorda di voi, voi non vi scordate della felicità” (R. Benigni)
-
niky
- novellino

- Messaggi: 6
- Iscritto il: 28/11/2011, 13:07
Re: Chelanti
Mi scuso in anticipo se faccio una domanda stupida ma a parte ossido di zinco e biossido di titanio che contengono chiaramente metalli nelle materie prime di base per formulare creme sono contenuti metalli per cui serve un chelante? grazie ciao
-
Lola
- Grande Capa

- Messaggi: 49357
- Iscritto il: 28/09/2006, 10:47
- Località: Monfalcone
Re: Chelanti
Sono contenuti negli strumenti che usiamo per emulsionare (pentole, lame del frullatore, cucchiaini). In realtà il chelante a noi non serve, difficile che un cosmetico vada rancido prima di un anno dalla produzione, e di solito ci riusciamo a consumarlo.
...perchè io VI VEDO
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
"Dovrei mettere all'ingresso del forum avete presente quei metal detector tipo negli aeroporti? Quando suona, faccio lasciare giù la scatoletta di bicarbonato e faccio passare solo senza."
-
pannina

- Spignattatrice

- Messaggi: 2928
- Iscritto il: 13/10/2011, 22:54
- Località: Genova
Re: Chelanti
Leggendo il topic sulla vitamina C mi son venuti dei dubbi... io uso il SAP nelle creme viso, sarebbe opportuno usare un chelante e se si quale più indicato? Io ho del trietiil citrato e del gluconolattone...
-
anto

- Spignattatore Esperto

- Messaggi: 5171
- Iscritto il: 03/10/2006, 9:54
Re: Chelanti
@Lola ... Però i chelanti potenziano l'azione del conservante e visto che gli spignatti con conservanti 'alternativi' sul forum abbondano è una sicurezza in più.
@Pannina, no. editronato di sodio, fitico o robe simili ...
@Pannina, no. editronato di sodio, fitico o robe simili ...
-
pannina

- Spignattatrice

- Messaggi: 2928
- Iscritto il: 13/10/2011, 22:54
- Località: Genova
Re: Chelanti
Beh... allora devo aspettare un nuovo ordine... 
Grazie Anto.
Grazie Anto.
-
pannina

- Spignattatrice

- Messaggi: 2928
- Iscritto il: 13/10/2011, 22:54
- Località: Genova
Re: Chelanti
Ce l'ho!  Magia mi ha donato una boccetta di editronato di sodio neutralizzato "kluben k2514"... è quello giusto? In che percentuale devo usarlo se ad esempio metto il 4% di SAP?
Magia mi ha donato una boccetta di editronato di sodio neutralizzato "kluben k2514"... è quello giusto? In che percentuale devo usarlo se ad esempio metto il 4% di SAP?
Anto?
Anto?